الکترون والانس چیست؟ کلید فهم رفتار شیمیایی و فیزیکی مواد
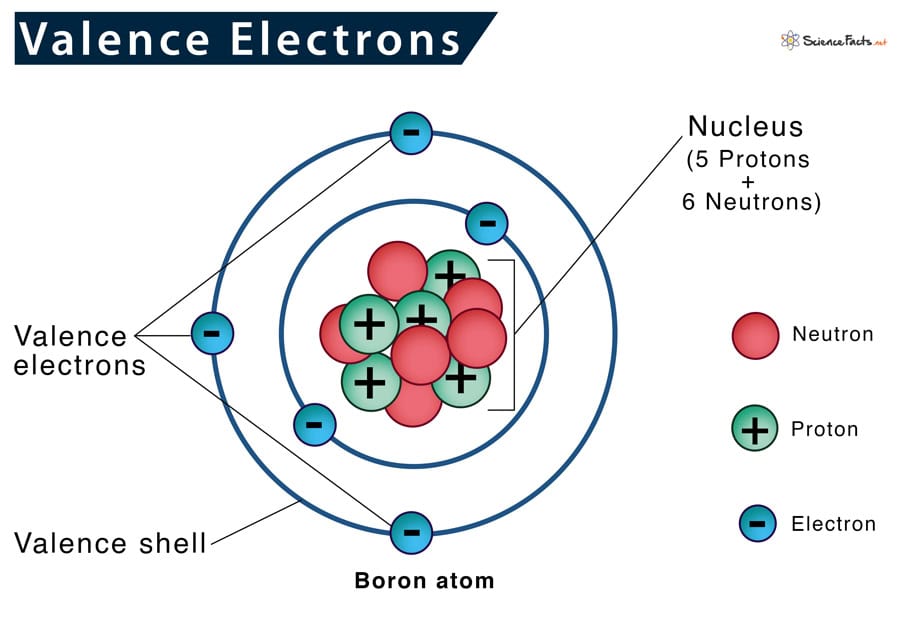
الکترون والانس به الکترونهایی گفته میشود که در بالاترین لایه انرژی (لایه والانس) یک اتم قرار دارند و در برهمکنشهای شیمیایی و فیزیکی اتم نقش کلیدی ایفا میکنند. این الکترونها به دلیل دوری از هسته و انرژی بالاتر، نسبت به الکترونهای داخلی (هستهای) راحتتر در واکنشهای شیمیایی، مانند تشکیل پیوندهای یونی یا کووالانسی، شرکت میکنند یا در فرآیندهایی مانند رسانایی الکتریکی نقش دارند. تعداد و توزیع الکترونهای والانس تعیینکننده خواص شیمیایی عناصر، مانند واکنشپذیری و توانایی تشکیل ترکیبات است. این مفهوم در شیمی، فیزیک و علوم مواد اهمیت اساسی دارد و پایهای برای درک رفتار عناصر در جدول تناوبی است. با بررسی الکترون والانس همراه ابرار صنعتی بمانید.
تعریف دقیق الکترون والانس
الکترونهای والانس بهطور دقیق، الکترونهایی هستند که در بالاترین پوسته انرژی (Principal Quantum Number, n) یک اتم قرار دارند و در اوربیتالهای s و p (و گاهی d یا f در عناصر واسطه) توزیع شدهاند. این الکترونها معمولاً در پیکربندی الکترونی اتم، آخرین الکترونهایی هستند که به اوربیتالها اضافه میشوند. برای مثال، در اتم کربن (1s² 2s² 2p²)، چهار الکترون در لایه دوم (2s² 2p²) الکترونهای والانس هستند. تعداد الکترونهای والانس معمولاً با گروه عنصر در جدول تناوبی مرتبط است و برای پیشبینی رفتار شیمیایی، مانند تشکیل پیوندها یا واکنشپذیری، استفاده میشود.
جایگاه الکترون والانس در مدل اتمی
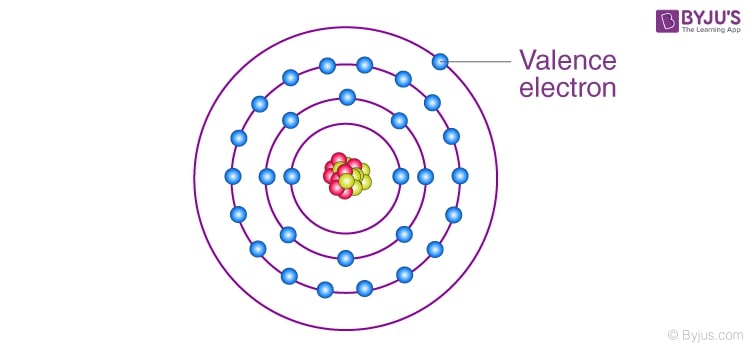
در مدل اتمی بور و مدل کوانتومی مدرن، الکترونهای والانس در بالاترین لایه انرژی (یا اوربیتالهای خارجی) قرار دارند و از هسته دورترند. در مدل بور، این الکترونها در مدارهای با شعاع بزرگتر حرکت میکنند و انرژی بالاتری دارند. در مدل کوانتومی، الکترونهای والانس در اوربیتالهایی با عدد کوانتومی اصلی بالاتر (n) قرار دارند، مانند 4s در پتاسیم یا 3p در فسفر. این جایگاه باعث میشود که الکترونهای والانس تحت تأثیر نیروی جاذبه هسته کمتری باشند و بهراحتی در فرآیندهای شیمیایی یا الکتریکی (مانند پیوند یا رسانایی) شرکت کنند. این الکترونها همچنین مسئول خواص طیفی اتمها هستند.
نحوه توزیع الکترونهای والانس در اوربیتالها
توزیع الکترونهای والانس در اوربیتالها بر اساس اصل آفبا (Aufbau)، قاعده هوند و اصل طرد پاولی انجام میشود. الکترونها ابتدا اوربیتالهای با انرژی پایینتر (مانند s) را پر کرده و سپس به اوربیتالهای p، d یا f میروند. برای مثال، در اتم اکسیژن (1s² 2s² 2p⁴)، شش الکترون والانس در اوربیتالهای 2s (دو الکترون) و 2p (چهار الکترون) توزیع شدهاند. قاعده هوند تضمین میکند که الکترونها ابتدا بهصورت تکتک در اوربیتالهای همانرژی (مانند 2p) قرار گیرند تا انرژی سیستم به حداقل برسد. این توزیع بر پیوندهای شیمیایی و خواص مغناطیسی اتم تأثیر میگذارد.
تفاوت الکترون والانس با الکترونهای هستهای
الکترونهای والانس در بالاترین لایه انرژی اتم قرار دارند و در برهمکنشهای شیمیایی شرکت میکنند، در حالی که الکترونهای هستهای (Core Electrons) در لایههای داخلیتر (با عدد کوانتومی اصلی پایینتر) قرار دارند و به هسته نزدیکترند. الکترونهای هستهای به دلیل جاذبه قویتر هسته، در واکنشهای شیمیایی بیاثر هستند و عمدتاً در پایداری ساختاری اتم نقش دارند. برای مثال، در سدیم (1s² 2s² 2p⁶ 3s¹)، الکترون 3s والانس است، اما ۱۰ الکترون دیگر (1s² 2s² 2p⁶) هستهای هستند. این تفاوت باعث میشود که الکترونهای والانس در رسانایی، پیوند و واکنشپذیری نقش داشته باشند.
روش تعیین تعداد الکترونهای والانس
برای تعیین تعداد الکترونهای والانس، از پیکربندی الکترونی یا شماره گروه در جدول تناوبی استفاده میشود. در عناصر گروه اصلی (Main Group Elements):
- گروههای ۱ و ۲ (مانند سدیم و منیزیم): تعداد الکترونهای والانس برابر با شماره گروه (۱ یا ۲).
- گروههای ۱۳ تا ۱۸ (مانند کربن یا اکسیژن): تعداد الکترونهای والانس برابر است با شماره گروه منهای ۱۰ (مثلاً گروه ۱۶: ۱۶-۱۰=۶).
برای عناصر واسطه، الکترونهای لایه s و گاهی d در نظر گرفته میشوند (مانند آهن: 3d⁶ 4s²، ۸ الکترون والانس). پیکربندی الکترونی از طریق طیفسنجی یا محاسبات کوانتومی تأیید میشود.
الکترونهای والانس و تأثیر آنها بر واکنشهای شیمیایی
الکترونهای والانس تعیینکننده رفتار اتمها در واکنشهای شیمیایی هستند، زیرا در تشکیل پیوندهای یونی، کووالانسی و فلزی نقش دارند. اتمها با به اشتراک گذاشتن، گرفتن یا دادن الکترونهای والانس به پیکربندی پایدار (مانند قانون هشتتایی) میرسند. برای مثال، اکسیژن (۶ الکترون والانس) با گرفتن دو الکترون از منیزیم، پیوند یونی تشکیل میدهد (MgO). در واکنشهای کووالانسی، مانند متان (CH₄)، کربن چهار الکترون والانس خود را با هیدروژن به اشتراک میگذارد. تعداد و انرژی الکترونهای والانس بر سرعت و نوع واکنشهای شیمیایی تأثیر میگذارد.
پیوند یونی و ارتباط آن با الکترون والانس
پیوند یونی زمانی رخ میدهد که اتمهایی با تفاوت الکترونگاتیوی زیاد، الکترونهای والانس را منتقل کنند. اتم با الکترونگاتیوی کمتر (مانند فلزات قلیایی) الکترون والانس خود را به اتم با الکترونگاتیوی بیشتر (مانند هالوژنها) میدهد، که منجر به تشکیل کاتیون و آنیون میشود. برای مثال، در NaCl، سدیم (۱ الکترون والانس) یک الکترون به کلر (۷ الکترون والانس) میدهد تا هر دو به پیکربندی پایدار گاز نجیب برسند. این انتقال الکترونهای والانس پیوند یونی قوی ایجاد میکند که در ترکیبات جامد مانند نمکها دیده میشود.
پیوند کووالانسی و سهمگیری الکترونهای والانس
پیوند کووالانسی زمانی شکل میگیرد که دو اتم الکترونهای والانس خود را به اشتراک بگذارند تا به پیکربندی پایدار برسند. برای مثال، در مولکول H₂O، اکسیژن (۶ الکترون والانس) دو الکترون را با دو اتم هیدروژن (هر کدام ۱ الکترون والانس) به اشتراک میگذارد و دو پیوند کووالانسی تشکیل میدهد. در مولکولهای پیچیدهتر مانند اتیلن (C₂H₄)، پیوندهای دوگانه از اشتراک چهار الکترون والانس بین اتمهای کربن ایجاد میشوند. نوع و تعداد الکترونهای والانس بر قدرت و قطبیت پیوندهای کووالانسی تأثیر میگذارند.
در فلزات، الکترونهای والانس (معمولاً ۱ تا ۳ الکترون در لایه s) در یک «دریای الکترونی» آزادانه حرکت میکنند و مسئول رسانایی الکتریکی و حرارتی هستند. این الکترونها به دلیل انرژی باند پایین و تحرک بالا، جریان الکتریکی را هدایت میکنند. برای مثال، مس (3d¹⁰ 4s¹) به دلیل یک الکترون والانس در لایه 4s، رسانایی بالایی دارد. تعداد الکترونهای والانس و ساختار بلوری فلز بر میزان رسانایی تأثیر میگذارد؛ فلزاتی با الکترونهای والانس بیشتر (مانند آلومینیوم) رسانایی متوسطی دارند. این ویژگی در طراحی هادیها و مدارها حیاتی است.
تأثیر تعداد الکترون والانس بر واکنشپذیری
تعداد الکترونهای والانس مستقیماً بر واکنشپذیری عناصر تأثیر میگذارد. عناصری با تعداد کم (۱ یا ۲) یا زیاد (۶ یا ۷) الکترون والانس، مانند فلزات قلیایی (Li, Na) یا هالوژنها (F, Cl)، به دلیل تمایل به رسیدن به پیکربندی پایدار گاز نجیب، بسیار واکنشپذیرند. برای مثال، فلوئور (۷ الکترون والانس) به شدت با گرفتن یک الکترون واکنش میدهد. در مقابل، عناصری با لایه والانس پر (مانند هلیوم با ۲ الکترون) بیاثر هستند. عناصر واسطه با الکترونهای d، واکنشپذیری متغیری دارند که به انرژی اوربیتالها بستگی دارد.
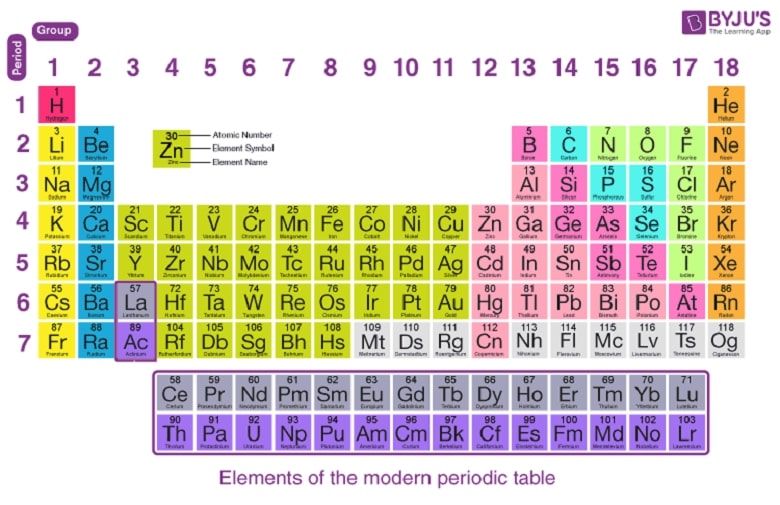
الکترون والانس و گروهبندی عناصر در جدول تناوبی
جدول تناوبی بر اساس تعداد الکترونهای والانس گروهبندی شده است. عناصر گروههای اصلی (۱, ۲, ۱۳-۱۸) تعداد الکترونهای والانس مشخصی دارند که با شماره گروه مرتبط است. برای مثال:
- گروه ۱ (فلزات قلیایی): ۱ الکترون والانس
- گروه ۱۶ (شبهفلزات): ۶ الکترون والانس
- گروه ۱۸ (گازهای نجیب): ۸ الکترون والانس (بهجز هلیوم با ۲)
عناصر واسطه (گروههای ۳-۱۲) ممکن است الکترونهای s و d را بهعنوان والانس داشته باشند.
رفتار الکترونهای والانس در نیمههادیها
در نیمههادیها، مانند سیلیکون و ژرمانیوم (۴ الکترون والانس)، الکترونهای والانس در باند والانس قرار دارند و با دریافت انرژی (مانند گرما یا نور) به باند هدایت منتقل میشوند. این انتقال امکان رسانایی الکتریکی را فراهم میکند. ناخالصیهایی مانند فسفر (۵ الکترون والانس) یا بور (۳ الکترون والانس) به نیمههادیها اضافه میشوند تا تعداد حاملهای بار (الکترون یا حفره) را افزایش دهند. رفتار الکترونهای والانس در نیمههادیها اساس کار ترانزیستورها، دیودها و سلولهای خورشیدی است و به طراحی مواد با رسانایی کنترلشده کمک میکند.
پیوند هیدروژنی و تأثیر الکترونهای والانس
پیوند هیدروژنی نوعی برهمکنش بینمولکولی است که در آن اتم هیدروژن (با ۱ الکترون والانس) که به اتم الکترونگاتیو (مانند اکسیژن با ۶ الکترون والانس) متصل است، با جفت الکترون غیرپیوندی اتم دیگر (مانند نیتروژن یا فلوئور) برهمکنش میکند. برای مثال، در آب (H₂O)، جفت الکترونهای غیرپیوندی اکسیژن پیوندهای هیدروژنی با مولکولهای دیگر ایجاد میکنند. این پیوندها، که به الکترونهای والانس وابستهاند، خواصی مانند نقطه جوش بالا و چگالی غیرعادی آب را توضیح میدهند.
در شیمی معدنی، الکترونهای والانس رفتار ترکیبات معدنی مانند اکسیدها، هالیدها و کمپلکسهای فلزی را تعیین میکنند. برای مثال، در اکسیدهای فلزی مانند Fe₂O₃، الکترونهای والانس آهن (3d⁶ 4s²) با اکسیژن پیوند یونی یا کووالانسی تشکیل میدهند. در کمپلکسهای هماهنگی، مانند [Co(NH₃)₆]³⁺، الکترونهای والانس فلز (کبالت) و لیگاند (آمونیاک) پیوندهای کووالانسی هماهنگی ایجاد میکنند. تعداد و توزیع الکترونهای والانس خواص مغناطیسی، رنگی و کاتالیزوری ترکیبات معدنی را تعیین میکنند.
کاربرد الکترونهای والانس در فناوری نانو
در فناوری نانو، الکترونهای والانس نقش کلیدی در خواص مواد نانوساختار دارند. برای مثال، در نقاط کوانتومی (مانند CdSe)، الکترونهای والانس در باندهای انرژی گسسته قرار دارند و خواص نوری مانند فلورسانس را تعیین میکنند. در نانولولههای کربنی، الکترونهای والانس کربن (2s² 2p²) رسانایی الکتریکی یا نیمهرسانایی را مشخص میکنند. کنترل تعداد و انرژی الکترونهای والانس در مواد نانویی، امکان طراحی حسگرها، کاتالیستها و قطعات الکترونیکی پیشرفته را فراهم میکند.
اثر دما و فشار بر انرژی الکترونهای والانس
دما و فشار میتوانند انرژی الکترونهای والانس را تغییر دهند. افزایش دما انرژی جنبشی الکترونها را افزایش داده و در نیمههادیها، الکترونهای والانس را به باند هدایت منتقل میکند، که رسانایی را بهبود میبخشد. در فشار بالا، فاصله بین اتمها کاهش یافته و همپوشانی اوربیتالهای والانس افزایش مییابد، که میتواند خواص فلزی یا عایقی مواد را تغییر دهد. برای مثال، تحت فشار بالا، کربن (گرافیت) به الماس تبدیل میشود، زیرا الکترونهای والانس در ساختار sp³ بازآرایی میشوند. این اثرات در طراحی مواد تحت شرایط سخت حیاتی است.
ارتباط بین ظرفیت شیمیایی و الکترون والانس
ظرفیت شیمیایی یک اتم، تعداد پیوندهایی است که میتواند با اتمهای دیگر تشکیل دهد و به تعداد الکترونهای والانس بستگی دارد. برای مثال، نیتروژن (۵ الکترون والانس) میتواند سه پیوند کووالانسی و یک جفت الکترون غیرپیوندی در NH₃ تشکیل دهد، که ظرفیت آن را ۳ نشان میدهد. در عناصر واسطه، مانند کروم (3d⁵ 4s¹)، ظرفیتهای چندگانه (مانند +۳ یا +۶) به دلیل مشارکت الکترونهای d امکانپذیر است. قانون هشتتایی و پیکربندی والانس رفتار ظرفیت را در ترکیبات پیشبینی میکنند.
مدلهای کوانتومی و توضیح الکترون والانس
در مدلهای کوانتومی، الکترونهای والانس در اوربیتالهایی با اعداد کوانتومی مشخص (n، l، m_l، m_s) توصیف میشوند. معادله شرودینگر انرژی و توزیع فضایی این الکترونها را پیشبینی میکند. نظریه پیوند والانس (VBT) رفتار الکترونهای والانس را در تشکیل پیوندهای کووالانسی توضیح میدهد، در حالی که نظریه اوربیتال مولکولی (MO) همپوشانی اوربیتالهای والانس را برای تشکیل باندهای پیوندی و ضدپیوندی بررسی میکند. نظریه میدان کریستالی (CFT) برای کمپلکسهای فلزی، نقش الکترونهای والانس d را در خواص مغناطیسی و طیفی توضیح میدهد. این مدلها درک دقیقی از رفتار شیمیایی و فیزیکی اتمها ارائه میکنند.